- PDF:PDF版をダウンロード
- DOI: https://doi.org/10.15108/stih.00221
- 公開日: 2020.08.25
- 著者: 伊藤 裕子
- 雑誌情報: STI Horizon, Vol.6, No.3
- 発行者: 文部科学省科学技術・学術政策研究所 (NISTEP)
ほらいずん
新型コロナウイルス感染症予防ワクチンの研究開発動向
感染者の行動や環境要因により感染の拡大を生じる新型コロナウイルス感染症(COVID-19)の世界的な流行は、人々の生活や社会経済活動に大きな影響を及ぼしている。そのため予防ワクチンが強く求められ、世界保健機関(WHO)は、世界中で進められている予防ワクチン候補の研究開発状況のリストを定期的に発表している。2020年7月24日発表のリストでは、人に対する臨床試験の段階に達しているワクチンのうち、DNAやRNAを利用する核酸ワクチンがもっとも多いことが示された。核酸ワクチンは予防ワクチンとしてまだ実用化されていないが、ワクチン作製の期間が従来よりも短くて済むなどの利点を持つ。また、論文分析より、核酸ワクチンの研究開発に関する論文はここ10年以上増加傾向にあることが示され、研究開発の知見が蓄積されつつあることが示唆された。
キーワード:COVID-19,予防ワクチン,臨床試験,核酸ワクチン
1. はじめに
2019年12月に中国の武漢市で流行が確認された新型コロナウイルス感染症(COVID-19)は急速に全世界に広がり、2020年3月11日に世界保健機関(World Health Organization, WHO)はパンデミック(世界的な大流行)の状態であると発表した。
飛まつ感染や接触感染を主な感染経路とするCOVID-19は、感染者の行動や環境要因により感染の拡大を生じ、症状は発熱や呼吸器症状等で多くは軽症であるが、高齢者や基礎疾患を持つ者は重篤化する可能性が高いと考えられている1)。2020年6月30日までに、世界の216の国・地域において確認された感染者数は1,000万例を超え、死亡数も50万例を超えたと報告された2)。日本国内では、2020年6月30日までに、感染者は約18,723人、死亡者は974人と報告された3)。現時点(2020年7月27日時点)でも、感染者・死亡者ともに増加し、終息の兆しがない。
したがって、人々が安心して社会活動や経済活動を行うためには、有効な治療薬や感染予防のためのワクチンが必要である。
治療薬としては、新型コロナウイルス(SARS-CoV-2)のRNA鎖の伸長反応を阻害する抗ウイルス薬(remdesivir)があり、重症患者に対して使用が認められている4)。しかし、インフルエンザの治療薬のように軽症者を含めて広く投与できる抗ウイルス薬はなく、予防ワクチンもない。
現在、予防ワクチンの研究開発は、世界中の企業や研究機関が急ピッチで進めている。本稿では、現時点でのCOVID-19予防ワクチンの研究開発動向について概説する。
2. COVID-19予防ワクチンの研究開発の状況
2-1 予防ワクチンの研究開発のプロセス
まず、医薬品の研究開発について解説する。医薬品開発(ワクチン含む)は、国際的協調が取られており、日本・米国・欧州各国などの先進国では、研究開発プロセスや安全性等の法規制は概ね共通する。
その研究開発は、基礎研究→前臨床試験(非臨床試験)→臨床試験(治験)→承認申請・審査というプロセスを経る。前臨床試験は、動物を用いて薬の有効性や安全性などを調べる研究段階である。臨床試験は、人に対する有効性や安全性などを調べる研究段階であり、その中にフェーズ1, 2, 3の3段階を含む。
医薬品は患者の治療を目的とするので、医薬品の臨床試験ではフェーズ1以外は患者を対象に実施される。一方、一般的にワクチンは健康人の予防を目的とする。したがって、感染症予防ワクチンの臨床試験では、すべての臨床試験のフェーズにおいて健康人の集団を対象に行う。フェーズ1は小規模、フェーズ2は接種量や接種回数及び接種経路等を明確にすることを目的に実施し、フェーズ3は大規模に実施し、ワクチンの有効性と安全性のデータを得る5)。臨床試験のフェーズの途中であっても、期待したような効果が得られなかった場合や、安全性に問題が発生した場合などは、その時点で臨床試験は中止になる。
2-2 COVID-19予防ワクチンの候補
(1)COVID-19予防ワクチンの候補と研究開発段階
WHOは、2020年7月24日付で、COVID-19の予防ワクチン候補の研究開発状況に関するリストを発表した6)。リストには、研究開発段階、ワクチンの種類、開発者などの情報が含まれた。
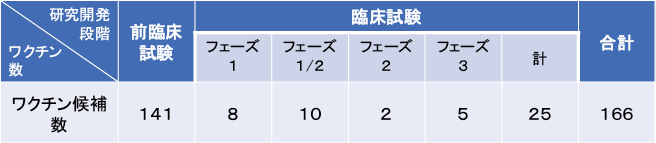
図表1に、予防ワクチン候補の研究開発段階についてまとめた。全166の予防ワクチン候補のうち、前臨床試験段階141候補、臨床試験段階25候補であった。そのうち臨床試験の最終段階であるフェーズ3に達しているワクチン候補は5候補、フェーズ2は2候補、フェーズ1/2(フェーズ1と2を続けて実施)は10候補、フェーズ1は8候補であることが示された。
(2)COVID-19予防ワクチンの種類
予防ワクチンは、あらかじめ免疫(抗体)を獲得することを目的として、病原体(ウイルス)そのものや一部を体内に入れることであり、感染症の発症を予防したり発症時の症状を軽減したりする。
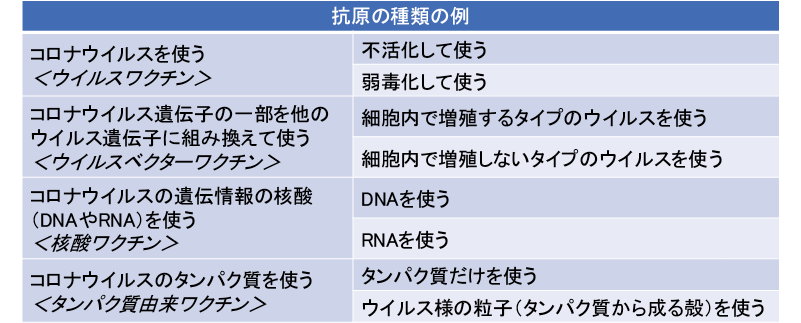
このときに体内に入れるウイルスなどの材料(抗原)は複数考えられ、COVID-19予防ワクチンの研究開発では少なくとも8種類のワクチン(抗原)が検討されている7)。これらは図表2に示すように、新型コロナウイルス本体の病原性を失わせたり弱めたりして用いるもの、新型コロナウイルスの遺伝子の一部を別のウイルスに遺伝子組み換えしてウイルスベクター(遺伝子の運び屋)として用いるもの、新型コロナウイルスの遺伝情報を含む核酸(DNA, RNA)を用いるもの、新型コロナウイルスのタンパク質を用いるものであり、大きく4種類に分けられる7)。これらの大部分は、遺伝子組み換え技術を利用している。
一般的にウイルスは、遺伝情報である核酸(DNAあるいはRNA)をタンパク質の殻(カプシド)で包むというシンプルな構造をとり、ウイルスによってはエンベロープという脂質と膜タンパク質から成る膜で更にカプシドを包んでいる8)。新型コロナウイルスは、遺伝情報としてRNAを持つウイルス(RNAウイルス)であり、エンベロープを有する。ウイルスの表面には外側に突き出たスパイクプロテインがあり、これを人の細胞表面に存在するACE2レセプターに接着させて細胞内に侵入し、そこでウイルスのRNAを放出する。ウイルスに侵入された人の細胞はウイルスRNAをタンパク質に翻訳し、それを基に人の細胞内でウイルスが再構成される7)。
したがって、COVID-19の感染にスパイクプロテインが重要な役割を果たすと考えられ、スパイクプロテインを含むウイルスの部分や、スパイクプロテインの遺伝子やタンパク質がワクチン(抗原)の材料として主に検討されている7)。
(3)COVID-19予防ワクチンの種類と研究開発状況
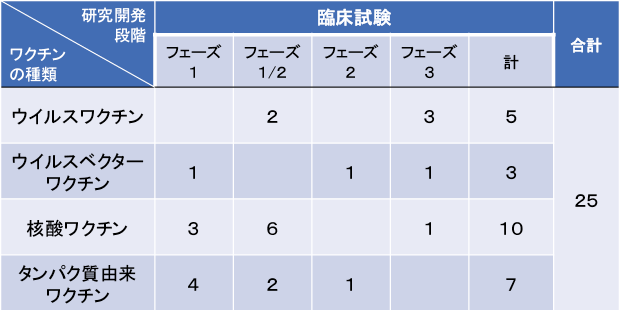
図表3には、WHO発表のワクチン候補リストに掲載された臨床試験段階の25の予防ワクチン候補をワクチンの種類別に分類し、研究開発段階ごとの候補数を示した6)。その結果、25の予防ワクチン候補のうち、最終段階のフェーズ3に達しているのはウイルスワクチン、ウイルスベクターワクチン、核酸ワクチンであり、中でも合計数では核酸ワクチンが10候補ともっとも多いことが示された。
ウイルスワクチンは現在多くの感染症予防に使用されているタイプのワクチンであるが、ウイルス本体を使用するので安全性の確保が重要であることや、通常、鶏卵を用いてワクチン製造をするため大量の鶏卵の準備や培養などワクチン製造過程に手間や時間が掛かる点に問題がある7)。
ウイルスベクターワクチン(組み換えウイルスワクチンともいう9))は、細胞内で増殖するタイプのウイルスベクターを用いたワクチンではエボラワクチン(2019年12月に米国で承認10))があり、細胞内で非増殖なウイルス(アデノウイルスなど)をウイルスベクターとして用いたワクチンはまだないが、遺伝子治療ではアデノウイルスベクターは長年利用されてきた7)。
タンパク質由来ワクチンは、新型コロナウイルスのスパイクプロテインや膜タンパク質といったタンパク質を投与するワクチンであるが、アジュバントという免疫を刺激する因子を併せて投与しないと免疫が生じないと考えられている7)。別のタンパク質由来ワクチンは、新型コロナウイルスの遺伝情報(RNA)の部分がない、殻のみのウイルス様粒子(VLP)であるので病原性がなく、かつ免疫応答はされるため期待されるが大量生産は困難と考えられている7)。
核酸ワクチンは、これまでのワクチンと大きく異なる。新型コロナウイルスの遺伝情報の一部のみ(スパイクプロテインに関するDNAやRNA)を人工的に合成し、これを人に投与することで、人の細胞内にウイルスのタンパク質を作らせて、免疫応答を生じさせるワクチンである7)。核酸ワクチンは、病原性がなく、かつ遺伝子情報や材料があれば容易に作ることができる。しかし、人に投与するワクチンとして使用が承認されたものはまだ存在していない。
DNAワクチンでは、遺伝子組み換えベクターであるプラスミドDNAにスパイクプロテイン遺伝子などを組み換えて人に直接投与するか、エレクトロポレーション法(電気せん孔法)によって細胞に入れる7)。プラスミドDNAに組み換えられたウイルス遺伝子(DNA)は人の細胞内でRNAに転写されてmRNAとなり、翻訳されてウイルスタンパク質ができ、これが抗原となる。
RNAワクチンでは、スパイクプロテインの遺伝情報が含まれるRNAを脂質で覆うなどして、人に投与する7)。人の細胞に入ったRNAはmRNAとして働き、この情報を基に翻訳されてウイルスタンパク質ができ、これが抗原となる。
2-3 COVID-19予防ワクチン候補である核酸ワクチン
(1)臨床試験段階の核酸ワクチン候補
既に臨床試験の研究段階に入っている核酸ワクチン候補の研究開発状況と研究開発実施機関を図表4に示した。
核酸ワクチン10候補のうち、DNAワクチンが4候補、RNAワクチンが6候補であった6)。研究開発実施機関からみると、Pfizer(ファイザー)以外はメガファーマ(巨大製薬企業)の参加がなく、中小企業やベンチャー企業が研究開発の主体であることが示唆された。

(2)核酸ワクチンの利点と懸念点
核酸ワクチンは、従来のワクチンとは異なる新しいタイプのワクチンであり、前項2-2にも示したように次のような利点がある。
● ワクチン製造にはウイルスの病原性部分を使用しない。
● ワクチンの製造期間が、従来のウイルスを培養するワクチン製造(通常1年以上かかる)に比べて大幅に短縮できる。
● 変異が速いウイルスであっても、遺伝情報がわかればその変異に対応して、迅速に新たなワクチンの作製ができる。
しかし、核酸ワクチンは人に対して使用が承認されたことがないワクチンであり、次のような懸念点がある。
◆ 感染予防に十分な免疫応答を生じて、それをある程度持続することができるか。
◆ 免疫応答を助けるために使用する適切なアジュバントがあるか、又は新たにアジュバントを研究開発することができるか。
◆ ワクチンの接種により、重篤な副反応(副作用のこと)が発生する可能性はないか。
3. 論文からみえる核酸ワクチンに関する研究開発動向
3-1 核酸ワクチンに関する論文件数の推移
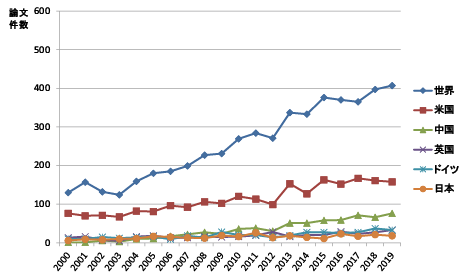
核酸ワクチンの研究動向について、論文分析を基に示した。論文データベース(Web of Science, Clarivate Analytics社)を用いて、世界全体と5か国ごとの論文数の推移を分析した。なお、5か国は、20年間(2000-2019年)の核酸ワクチンに関する論文数の合計が上位5位の国を選んだ。
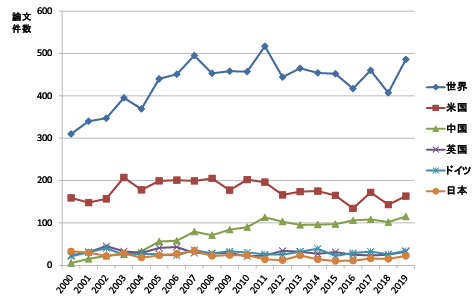
図表5に示すように、全体(世界)の傾向は、DNAワクチンに関する論文数では、2005年以降から大きな増減はなくほぼ一定の推移(図表5(a))を示し、RNAワクチンに関する論文数では、2004年以降に増加(図表5(b))を示した。
国別では、DNAワクチン及びRNAワクチンのどちらに関しても米国の論文数がもっとも多く、次いで中国であった。DNAワクチンの論文では、米国と中国の論文数の差は小さく、米国では2011年以降に論文数が減少し、中国ではほぼ一定数を推移していることからその差は更に小さくなることが予想された。RNAワクチンの論文に関しては、米国及び中国の論文数の差はやや大きいが、2015年以降に米国の論文数はほぼ一定となり、一方中国の論文数は緩やかに増加しているので、米国と中国の論文数の差は次第に小さくなると考えられる。
また、RNAワクチンの論文では、世界の論文数の増加状況が5か国を合わせた増加状況に比べて急激であった。分析したところ、5か国以外の複数の国で、近年論文数が増えていることが示された。
以上より、核酸ワクチンについての研究開発の知見が急速に蓄積されつつあることが示唆された。
3-2 核酸ワクチンに関する被引用回数のトップ論文
近年(2016-2019年)に発表された核酸ワクチンに関する論文を、前述の論文データベース(Web of Science)を用いて同様な検索ワード等で検索した結果、DNAワクチンの論文は1,770件、RNAワクチンの論文は1,539件であった。
これらの論文のうち、被引用回数がもっとも多い論文を調べたところ、DNAワクチンでは「Vaccine protection against Zika virus from Brazil (Nature, vol. 536, 474–478, 2016)」で被引用回数278回、RNAワクチンでは「Zika virus protection by a single low-dose nucleoside-modified mRNA vaccination(Nature, vol. 543, 248–251, 2017)」で被引用回数230回であることが示された。
両論文とも内容は、ジカウイルスによる感染症の予防ワクチンの研究開発についてであり、動物実験での効果を示した。ジカウイルス感染症は蚊を媒介し、妊婦が感染すると胎児に重大な影響を与える感染症であり、2015年には南米やカリブ海地域の20の国や地域で流行した11)。
残念ながら、ジカウイルス感染症予防のための核酸ワクチンはまだ実用化されていない。しかし、WHO発表のワクチン候補リストに掲載された研究開発実施機関には、ジカウイルス感染症の核酸ワクチン開発の実施機関が複数含まれている。このことはCOVID-19予防ワクチンの研究開発に、ジカウイルス感染症のワクチン開発の知見が活用されていることを示唆すると考えられる。
4. おわりに
本稿は、2020年7月27日時点に公表されたデータに基づいて解説を試みたものである。COVID-19予防ワクチンに関する研究開発は加速しており、時々刻々と状況が変化していることに注意されたい。
参考文献・資料
1) 国立感染研究所 感染症疫学センター,<注目すべき感染症>新型コロナウイルス感染症(COVID-19),IDWR 2020年第23号
2) World Health Organization (WHO), Coronavirus disease (COVID-19) pandemic
https://www.who.int/emergencies/diseases/novel-coronavirus-2019(2020.7.1 アクセス)
3) 厚生労働省,新型コロナウイルス感染症の現在の状況と厚生労働省の対応について(7月1日版),2020年7月1日発表.
https://www.mhlw.go.jp/stf/newpage_12177.html(2020.7.9アクセス)
4) 独立行政法人医薬品医療機器総合機構(PMDA)の「医療用医薬品 情報検索」を用いて、疾患名等により検索を行い、得られた医薬品添付文書等の情報から記載。
https://www.pmda.go.jp/PmdaSearch/iyakuSearch/(2020.7.10アクセス)
5) 厚生労働省,「感染症予防ワクチンの臨床試験ガイドライン」について(薬食審査発0527第5号),平成22年5月27日発表.
6) WHO, Draft landscape of COVID-19 candidate vaccines, 2020.7.24.
https://www.who.int/publications/m/item/draft-landscape-of-covid-19-candidate-vaccines (2020.7.27アクセス)
7) Ewen Callaway, The race for coronavirus vaccines, Nature, Vol.580: 576-577, 2020.
8) ウイルスを知る,ひと目でわかるウイルスと病気,Medical Tribune, Special Edition, 2-4, 2014年12月9日版.
9) 感染症の予防を目的とした組換えウイルスワクチンの開発に関する考え方,「異種抗原を発現する組換え生ワクチンの開発における品質/安全性評価のありかたに関する研究」総合報告書(研究代表 山口照英),平成 29 年度 厚生労働行政推進調査事業,2017.
10) FDA (U.S. Food and Drug Administration), First FDA-approved vaccine for the prevention of Ebola virus disease, marking a critical milestone in public health preparedness and response, FDA NEWS RELEASE, 2019.12.19発表.
11) ジカウイルス感染症とは,国立感染症研究所
https://www.niid.go.jp/niid/ja/kansennohanashi/6224-zika-fever-info.html (2020.7.16アクセス)